
当地时间10月5日,在瑞典首都斯德哥尔摩卡罗琳医学院,诺贝尔奖委员会总秘书长托马斯·佩尔曼宣布,2020年诺贝尔生理学或医学奖授予哈维·阿尔特(Harvey J. Alter),迈克尔·霍顿(Michael Houghton)和查尔斯·M·赖斯(Charles M. Rice),以表彰他们在“发现丙型肝炎病毒”方面作出的贡献,三位获奖者将分享1000万瑞典克朗奖金(约合760万人民币)。
哈维·阿尔特 (Harvey J. Alter),美国病毒学家,出生在纽约市,1956年在罗彻斯特大学获得文学学士学位,1960年在该校得到医学学位。1964年与后来的诺贝尔奖得主巴鲁克·塞缪尔·布隆伯格发现了澳大利亚抗原,后来被认为是乙肝病毒的一部分。他还以动物模型来研究人体免疫缺陷病毒,并确定了丙型肝炎病毒。2000年获拉斯克临床医学研究奖,2013年获盖尔德纳国际奖。
迈克尔·霍顿(Michael Houghton),英国生物化学家,参与开发丙型肝炎测试。霍顿1972年获东英吉利大学学士学位,并于1977年获伦敦大学国王学院生物学博士学位。然后,他在白金汉郡塞尔研究实验室工作,在1982年成为希龙公司的非甲非乙型肝炎部主管。
查尔斯·M·赖斯(Charles M. Rice),美国病毒学家,其主要研究领域是丙型肝炎病毒。他是洛克菲勒大学的病毒学教授。他与Ralf F. W. Bartenschlager和Michael J. Sofia共同获得了2016年拉斯克-狄贝基临床医学研究奖。

因新冠肺炎疫情,本次活动诺贝尔委员会对人数也进行了严格控制,会场不超过30人。(总台记者 郝晓丽)
长文解析最新诺奖研究:一年杀死40万人的致命传染性,即将迎来末日?
在刚刚公布的2020年诺贝尔生理学或医学奖中,美国病毒学家哈维·詹姆斯·奥尔特(Harvey James Alter)、英国生物化学家迈克尔·霍顿(Michael Houghton)及美国病毒学家查尔斯·M·赖斯(Charles M. Rice)因发现丙型肝炎病毒而获奖。从奥尔特发现“非甲,非乙”肝炎,到霍顿在1989年确定丙型肝炎病毒,再到赖斯证明这种病毒能够引起肝炎,这三位科学家以及其他研究者的一系列工作,让我们认识到这种致命疾病,并有机会寻找治疗方案。在丙肝病毒发现之后的30年间,对于丙肝病毒的研究出现了哪些令人惊喜的成果?我们距离消灭丙肝还有多远?在《环球科学》2017年9月刊的《丙肝末日已至》一文中,法国博戎医院肝病科主任帕特里克·马塞林等人为我们介绍了人类对抗丙肝病毒的最新战况。
更多关于获奖者及获奖研究的介绍,请点击:
刚刚,诺贝尔生理学或医学奖揭晓!3位英美科学家因发现丙肝病毒获奖
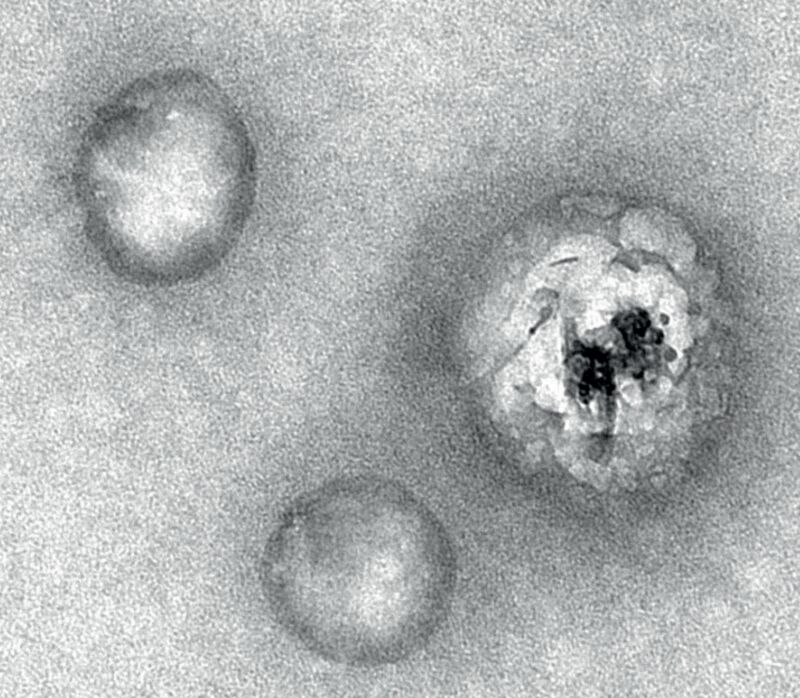
丙型肝炎病毒的电镜照片
撰文 | 帕特里克·马塞林(Patrick Marcellin)、
皮尔·卡尔迪(Pierre Kaldy)
翻译 | 徐寒易
丙型肝炎是肆虐全世界的瘟神。这种疾病是由一种攻击肝细胞的病毒导致的,患者在经历了数十年的慢性感染后会患上肝硬化,有时会发展成肝癌。继乙型肝炎之后,丙型肝炎是全世界第二大会导致癌症而致人死亡的传染病。
根据世界卫生组织的数据,在2015年,丙型肝炎造成40万人死亡,其中15万人死于肝癌。世界卫生组织还表示,由于数据缺失,丙型肝炎造成的实际死亡人数要超过上面的数字。自2012年起,丙型肝炎在美国成了头号致死传染病,许多人死于丙型肝炎导致的肝癌或与肝硬化有关的肝功能衰竭;死于丙型肝炎的人数比包括艾滋病、结核病在内的其他60种传染病的致死人数加起来还多。人类将要迎来丙型肝炎的死亡率高峰,因为根据世界卫生组织的数据,目前全世界有7100万人患有慢性丙型肝炎。丙型肝炎和酒精中毒是全世界肝脏移植手术的主要原因。
由于大部分患者对自己的病情一无所知,控制丙型肝炎的任务非常棘手。我们估计,在那些患有慢性丙型肝炎的人群中,只有20%的人知道自己被感染了。雪上加霜的是,并不是所有丙型肝炎患者都会出现症状。而一旦丙型肝炎病毒在人体内落地生根,这种慢性病可以在人体内潜伏几十年,然后才会首次出现肝脏损伤的症状。
抓住神秘病毒
不过,现在染上丙肝已不意味着前景凄凉了。这在之前还完全无法想象,但如今我们已经可以在几周内治好大部分丙肝患者了,即使晚期患者也不在话下。这个成就要归功于药物研究领域的一系列突破:研究人员搞清楚了丙型肝炎病毒的结构,成功在体外重现了它们的感染过程,而且还找到了针对病毒在人体内增殖所需的酶的药物。
人们对丙肝的认识始于20世纪70年代末。当时,一些医生发现了一种新的通过输血感染的慢性肝炎。导致这种肝炎的既不是甲型肝炎病毒,也不是乙型肝炎病毒。在之后的10年里,生物学家一直尝试从患者体内将这种肝炎病毒分离出来,但一无所获。1989年,美国凯龙(Chiron)制药公司的迈克尔·霍顿(Michael Houghton)领导的研究团队借助一种新的分子生物学技术,终于识别出了丙型肝炎病毒。

迈克尔·霍顿
由于无法提纯血液中的丙型肝炎病毒颗粒,也无法在体外培养,霍顿等人转而尝试直接分离血液中的病毒基因组。他们用一只受感染的黑猩猩的血液(血细胞已被清除),建立起了一个遗传物质库,然后把这些基因片段植入100万个噬菌体(攻击细菌的病毒)中。被这些噬菌体感染的细菌,就能够合成目标病毒的蛋白质片段。
另外,他们又获得了一个已经对神秘病毒产生抗体的患者的血清样本。在和上述细菌接触后,血清中的抗体识别出了由细菌表达的病毒蛋白片段。利用这种方法,他们终于追溯得出了编码这些蛋白的病毒基因序列。通过这些当时刚刚诞生的技术,霍顿的团队理清了病毒基因组的几乎所有序列。
变化多端
丙型肝炎病毒基因组被破译后,科学家发现原来这是一种属于黃病毒科(Flaviviridae,寨卡病毒和登革热病毒都属于此科)的小型RNA病毒,而且它们仅仅编码10种蛋白质。至此,研究人员终于可以研究这些蛋白质了,这也是让病毒失活的第一步。研究者对感染进程中产生的病毒进行基因测序后发现,丙型肝炎病毒还有一个不为人所知的可怕特点:超强的变异性。和丙型肝炎病毒一样,另一种小型RNA病毒——艾滋病毒也具有这种性质。超强的变异性使得丙型肝炎病毒能够绕过免疫系统的识别机制,这让疫苗的研制变得更加棘手。
因为病毒都非常小,所以它们可以在肝细胞内快速复制。我们估计,一个感染者体内每天都会复制产生1万亿个新病毒,而这些病毒之间还存在细微的差异。面对病毒的庞大数量和变异性,宿主的防御机制很快就溃败了。为了让免疫系统重整旗鼓,清除那些受感染的肝细胞,必须要找到能阻止病毒无休止复制的方法。一开始,研究人员拿丙型肝炎病毒一点办法也没有,因为无法在体外的肝细胞中培养这些病毒。此外,研究人员仅在一种模式动物——黑猩猩身上,重现了丙型肝炎病毒的感染过程。
不过,在研究病毒复制的过程中,研究者有了两个令人振奋的发现。首先,丙型肝炎病毒主要感染肝脏,药物很容易通过口服的方式到达这个器官。其次,与乙型肝炎病毒及艾滋病毒不同,丙型肝炎病毒只存在于细胞质中,不会常驻在细胞核或者细胞的基因组中。由于这两个特点,我们有可能在人体内彻底清除丙肝病毒。本文作者帕特里克·马塞林在1997年证实了这一点,他用一种小型抗病毒蛋白质——干扰素α(IFN-α)对一些丙型肝炎患者进行了几个月的治疗,并治好了他们。
1986年,美国的肝脏疾病专家注意到,一些丙型肝炎患者在每周注射3次IFN-α,连续注射一年后,病情消失了。IFN-α这种蛋白质来源于人体自身,它能够刺激被病毒感染的免疫系统。从那时开始,科学家开始用基因工程技术制造这种蛋白质。马塞林在1997年进行的那项研究显示,在用该蛋白质进行治疗后,一些患者肝脏和血液内的丙型肝炎病毒彻底消失了。
1999年,终于有一个大发现打开了丙肝病毒研究的局面。德国美茵茨大学的拉尔夫·巴腾史拉格(Ralf Bartenschlager)的团队宣布,他们实现了丙型肝炎病毒基因组在细胞中的稳定复制。该团队发现,如果仅将部分病毒基因组引入人类肝癌细胞中,那么病毒就会自动开始复制。
在体外成功复制病毒,给了医药产业仔细研究丙型肝炎病毒和测试各类阻断药物的契机。但直到2005年,在一个日本患者体内发现了一类特殊的丙肝病毒后, 研究者才在体外重现了病毒在人体肝细胞内的完整感染周期。该病毒能够避开细胞内部的抗病毒机制,毒性超强。不过,早在得到病毒的完整模型之前,研究者就开始测试不同的抗病毒方法了。
他们找到的第一个靶点是NS3,这是病毒基因组编码的一种重要蛋白质。丙型肝炎病毒的遗传物质是一个特殊的RNA分子,能编码一种长链前体蛋白,这种前体蛋白是由10种病毒蛋白构成的。其中的NS3是一种蛋白酶,可以分解部分长链前体蛋白,从而把一些成熟的病毒蛋白释放出来。1996年,病毒学家得到了这种蛋白酶的晶体,从而得以更细致地研究它的结构。NS3在当时看来是一个完美的靶点,而且研究者可以参考此前艾滋病毒的研究经验。
艾滋病毒也能产生一种蛋白酶,而抑制这种酶的药物沙奎那韦(saquinavir)的疗效相当出色。这种药物是得益于计算机建模的进步,在1995年开发出来的。由于沙奎那韦对艾滋病效果极佳,在上市后的第二年,也就是1997年,美国死于艾滋病的人数就下降到了此前的三分之一。这种药物标志着艾滋病鸡尾酒疗法黄金时代的到来。鸡尾酒疗法联合使用几种抑制病毒复制的口服药物,病人对这些药物也有较好的耐受性。
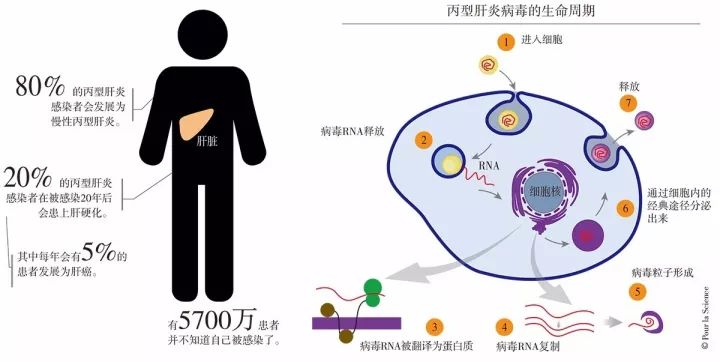
病毒的感染机制:
丙型肝炎病毒是通过血液或者被血液制品污染的医疗设备感染的。如果人体不能一次性消灭丙型肝炎病毒(大约20%的感染者是这种情况),那么病毒就会在肝脏里无声无息地定居下来,导致慢性感染和肝脏纤维化。不过,慢性丙型肝炎是可诊断的,只需检验血液中是否含有病毒的RNA基因组即可。在经历了约20年的慢性丙型肝炎病程后,约20%的患者最后会发展成肝硬化,而其中每年有5%的患者会患上肝癌,而这背后的机制尚不明朗。
病毒会把肝脏向血液输出的脂质颗粒当作“特洛伊木马”,向身体各处传播并感染其他细胞。这些颗粒会和细胞膜上的某个受体结合,并通过内吞作用(endocytose)进入细胞。内吞作用是细胞汲取营养的一种机制,而遇到携带着丙型肝炎病毒的脂质颗粒时,细胞膜会凹陷,将其整个包裹起来形成一个小囊泡,接着这个小囊泡和细胞膜分离,将病毒粒子运送到细胞内部(1)。
护送病毒的脂质颗粒的包膜和小囊泡的膜融合,使病毒RNA被释放到细胞内(2)。接着,病毒RNA被翻译为蛋白质(3)。其中的一些蛋白质会在细胞膜上复制病毒RNA(4)。当病毒RNA和蛋白质累计到一定程度时就会形成新的病毒(5),接着通过肝细胞的经典脂质颗粒分泌途径被分泌(6)或释放(7)出来。
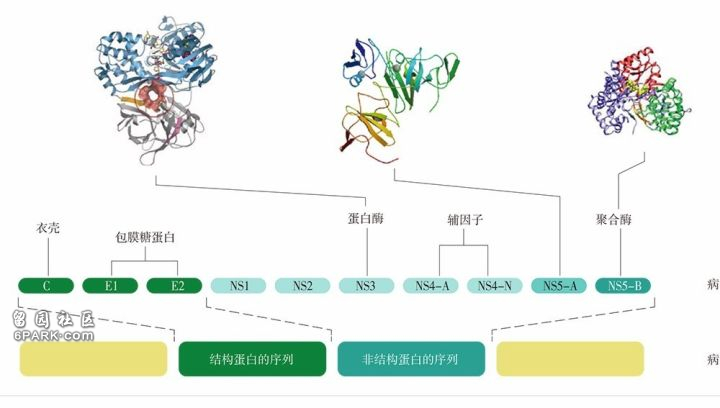
病毒基因组编码了10种蛋白质,其中3种属于结构蛋白,可以组装病毒的衣壳,将病毒包裹起来;另外7种蛋白质的功能是复制病毒。丙型肝炎病毒有7个基因型,不同基因型的基因序列之间的差别至少有30%,而且还有不少基因亚型存在,亚型间的序列差别也有20%。在一个丙型肝炎患者体内,每个病毒粒子均略有不同,因为病毒基因组的复制并不完美忠实于原版。每天患者体内都会产生数以千计的丙型肝炎病毒准种(quasispecies,由一系列相关的基因型组成的群体)。
要想在细胞内阻断病毒活性的话,目前有3类直接作用于病毒的抗病毒药物。一类以蛋白酶NS3为靶点(但有时也会与辅因子NS4-A结合);第二类以蛋白质NS5A为靶点;第三类以聚合酶NS5B为靶点。
丙型肝炎病毒的首个抑制剂
不过,对丙型肝炎病毒的研究遇到了一个始料不及的障碍。研究者通过生物信息技术分析了NS3蛋白质的立体结构,发现这种分子没有任何可供抑制剂结合的“口袋”结构。因此有许多研究者转而开始寻找其他病毒蛋白质来充当药物靶点。然而,加拿大勃林格殷格翰制药公司(Boehringer Ingelheim)的化学家蒙特斯· 林纳斯·布鲁内特(Montse Llinas Brunet)领导的团队却决定坚守阵地。2003年,该团队合成了一种能够阻断NS3的分子。这种分子非常稳定,体积也小,因此可以通过口服吸收。初步临床测试结果非常理想,服用了这种名为BILN 2061的药物后,病人血液中的病毒载量下降到了原来的千分之一,几乎无法被检出。和同时代的其他疗法相比,这是前所未闻的。
同时代的其他疗法主要依赖每周一次,连续24周或48周的IFN-α皮下注射,并且要搭配一种口服的抗病毒小分子药物利巴韦林(Ribavirin,可以增强IFN-α的疗效,机制未知)。不过,这类疗法非常昂贵,而且耐受性不良。接受这类疗法6个月后,如果病人的血液中无法检出病毒,那么就可视为痊愈。病人能否痊愈取决于病毒株(病毒的基因型)以及血液中的病毒载量。IFN-α疗法对于基因2、3型的丙型肝炎病毒比较有用,但是对于基因1型的效果就差强人意了。基因1型是西方世界最常见的病毒株,仅有不到一半的被基因1型病毒感染的患者能用IFN-α疗法治愈。
而BILN 2061这种NS3蛋白酶抑制剂对基因1型病毒感染相当有效。由于可以特异性阻断NS3,所以BILN 2061不仅能阻碍丙型肝炎病毒的复制,还能阻止NS3蛋白酶对细胞防御机制的破坏。另外,和IFN-α相比,BILN 2061的副作用更少。IFN-α常会引发流感样症状,比如疲劳、抑郁、焦虑、失眠,联合使用的药物利巴韦林有时还会导致贫血。
其他一些实验室也跟风制造出了一系列新的NS3抑制剂,其中两种在2011年上市,分别叫做特拉匹韦(Telaprevir)和博赛泼维(Boceprevir)。不管怎么说,光靠这3种口服新药还不足以根治丙型肝炎,因为这种病毒变异性太强,只需一个突变它就可以绕过药物的阻断。此外,这3种药物和许多药物不能共用,而且也有一些副作用。不过,如果将这3种药与旧疗法(IFN-α和利巴韦林)结合起来,就可以显著增加基因1型的治愈率,甚至可以挽救那些旧疗法无效的患者。
这是丙型肝炎病毒第一次在一种以它的某个成分为靶点的简单药物面前屈服。这些特异性抑制剂强大的疗效说明,对具有多重角色的病毒蛋白进行阻断,能够起到事半功倍的抗感染效果。直接作用抗病毒药物(Direct-acting antiviral,DAA)的时代已经到来,药物研发者开始了一场阻断其他病毒蛋白的竞赛,并带来了新的惊喜。
抗病毒武器库
另一个得到充分研究的靶点是NS5B,这是一种聚合酶,可帮助病毒基因组进行复制。和NS3一样,NS5B也是病毒的非结构蛋白(这种蛋白质不是成熟病毒颗粒的一部分,但在病毒复制和组装过程中发挥着重要作用),而且人体细胞中也不含类似蛋白质。1999年,科研人员分离、提纯了NS5B,并制作了这种蛋白的晶体,搞清楚了它的立体结构,发现NS5B上有不少可供抑制剂结合的潜在位点。因为之前对艾滋病毒逆转录聚合酶结构的研究极大推动了艾滋病药物的研发,因此,一些制药企业在知晓了NS5B的研究结果后,开始了科研竞赛,争相寻找不容易让丙型肝炎病毒出现耐药性的抑制剂,它们的具体方法是在体外测试耐药病毒株的出现速度。
2004年,第一种抑制剂出现了,它可以阻止丙肝病毒利用NS5B聚合酶合成RNA。因为这种抑制剂结合的目标是NS5B上的一个活性位点,所以它对所有病毒株都有效。另外,那些能够阻止抑制剂发挥作用的突变会严重干扰NS5B聚合酶的功能,以至于病毒无法正常复制。2010年,另外一种同类抑制剂也登场了,它叫做索非布韦(sofosbuvir),是由美国初创公司Pharmasset的迈克尔·索菲亚(Michael Sofia)团队研发的。Pharmasset在2011年被吉利德科学公司(Gilead)收购。
2012年,索非布韦的第一批临床试验结果出来了。联合使用利巴韦林的话,该抑制剂不但对基因2、3型疗效显著,而且病人的耐受性也很好。更理想的是,每天只要服用一剂就能见效,而且这种抑制剂和其他药物也兼容,这就极大地扩展了可治愈患者的基数。
2013年,由于索非布韦的临床试验结果十分喜人,美国食品及药品管理局(FDA)批准了使用该药物的疗法。在27年的研究之后,这是我们第一次不使用IFN-α就能治愈一些丙型肝炎患者。
与此同时,研究人员开始把目光投向另外一种丙型肝炎病毒蛋白——NS5A,因为他们注意到该蛋白的突变能够阻止病毒感染细胞。不过想要阻断NS5A是非常困难的,因为当时研究者甚至还不清楚这种蛋白质的具体功能(我们现在已经知道,它能够调节病毒的复制和组装)。2010年,美国制药公司百时美施贵宝(Bristol-Myers Squibb)的一个团队宣布研发出了一种针对NS5A的特异性抑制剂。
该团队在体外测试中,对100万种有望抑制病毒复制的分子进行了海选。接着,研究人员又从筛选出来的分子中,排除了那些会抑制NS5A以外的酶的分子——剩下的分子只能阻断NS5A,从而抑制病毒的复制。然后,该团队对其中一种分子的结构进行了调整,改善了它的吸收效果以及药理特性。他们努力的结果就是目前为止对丙型肝炎病毒最有效的药物达卡他韦(daclatasvir)。实际上,第二年的临床试验证实,病人对达卡他韦的耐受性良好,而且达卡他韦能够将患者血液中的病毒浓度降低到不足原来的千分之一(而剂量仅是BILN2061的四分之一)。2012年,这个精确打击丙型肝炎病毒的新型武器终于登场了,它的抗感染药效前所未有。现在要做的就是在更多的患者身上进行测试。
直接作用抗病毒药物(DAA)的出现,为对抗丙型肝炎的战斗带来了新的希望——人类有望在不使用IFN-α和利巴韦林的情况下彻底根除所有患者体内的丙型肝炎病毒。2012年,在旧疗法完全无效的患者身上进行的首次临床试验,让这种希望更加接近现实。医生们联合使用达卡他韦和另一种NS3抑制剂,在3个月的疗程后成功治愈了11名患者中的4人。这是人们首次通过口服治疗的方式治愈丙型肝炎。
第二年,在对近百人进行的临床试验中,一种联合使用达卡他韦和索非布韦的疗法在24周内治愈了90%以上的患者,其中一些是所有旧疗法均无效的顽固性患者,并且已经进入了肝硬化晚期。这种疗法不仅对基因1型有效,对基因3、4型也起了作用,这可是闻所未闻的结果。
2013年,索非布韦获批与传统疗法联合使用治疗丙型肝炎,成为了第三种正式上市的DAA药物。与此同时,欧洲和美国的医疗专家、药物研发实验室和药品监管机构之间深入合作,开展了一系列大规模临床试验,来确定最有效的DAA药物和针对不同病人的最佳药物组合。
2014年,丙型肝炎治疗领域迈出了决定性的一步——欧洲和美国批准了首个不使用IFN-α和利巴韦林的疗法。这种疗法联合了两种DAA药物:索非布韦和雷迪帕韦(ledipasvir)。雷迪帕韦是另一种NS5A抑制剂。这种疗法的耐受性优良,而且对于基因1型特别有效,只要连续12周口服即可。目前的丙型肝炎治疗主要用的就是这种疗法。
目前,在美国和欧洲共有5种联合使用NS3、NS5A以及NS5B抑制剂的疗法得到了批准,未来几年还将出现其他疗法。联合索非布韦和其他DAA的疗法可以治疗全世界所有基因型的丙型肝炎病毒。另外,这些新药甚至对晚期肝硬化也有效,因此有助于减少需要肝移植的患者数量。还有,它们对接受了肝移植的患者也有用。移植肝脏的患者需要接受免疫抑制治疗,以降低免疫系统对移植肝脏的排异反应,但这会促使病毒再次感染移植的肝脏,这也是肝移植失败的主要原因,而上述药物能够防范这种问题。丙型肝炎病毒导致的肝硬化会严重损害肝功能,病毒被药物清除后,患者的肝功能也有所恢复。现在,有超过95%丙型肝炎患者可以完全治愈。而新的疗法(联合使用现有的或新的抑制剂的疗法)正式推出后,还将刷新这个数字,因为第一批临床试验结果显示,这些新疗法能够对付所有病毒株,不管病毒是什么基因型。
这些新疗法将给丙型肝炎的治疗,以及在公共卫生的层面上控制丙型肝炎带来革命性的变化。病人可以在家服药,并且只需到特殊治疗中心接受病情监控即可。在治疗后的3个月,如果血液中检测不出病毒载量,那么基本不会复发。在专家眼中,有了这些进步,我们有可能在整个国家消灭丙型肝炎。那些容易感染丙型肝炎的边缘人群,比如注射吸毒者、囚犯以及艾滋病毒感染者将有更多机会接受治疗。比如,根据法国公共卫生监控研究所(Institut de veille sanitaire)的估计,在2011年法国有19.3万人感染丙型肝炎病毒,其中大约有65%是注射吸毒者,5%是囚犯,18%是艾滋病毒携带者。
消灭丙型肝炎
我们与丙型肝炎的战争已经结束了吗?切莫高兴得太早,实际上还有几个难题有待攻克。首先就是要筛查出数量庞大、还没意识到自己染病的慢性丙型肝炎患者。DAA是他们的福音,因为药物可以治好丙型肝炎带来的疲劳乏力、肌肉关节酸痛,使他们的生活质量得到大幅度改善。另外,对慢性丙型肝炎患者的研究显示,丙型肝炎病毒常会使人体产生胰岛素抵抗,患上糖尿病,同时增加心脑血管疾病的风险。丙型肝炎还会诱发一些癌症,如胆道癌、弥漫性大B细胞淋巴瘤。2016年末,一种更廉价的便携诊断方法得到了世界卫生组织的认证,这标志着大规模丙型肝炎筛查已迈出了第一步。
第二个难题就是施行上述疗法所需要的大规模资金支持。目前这些疗法还过于昂贵,尤其是对于那些深受丙型肝炎困扰的发展中国家而言。不过,由于预见到药物价格将会下降,并且疗程将缩短至8周甚至更短,包括法国、德国、葡萄牙、苏格兰、澳大利亚、爱尔兰在内的几个国家已经表明了在10年内消灭丙型肝炎病毒的决心。
法国卫生部部长在2017年4月宣布,新的疗法将在所有丙型肝炎患者中普及,而此前只有出现了晚期症状(肝硬化前期,肝纤维化终末期),或者那些有较高病毒传播风险的患者才能够接受新疗法的治疗。
从世界范围来看,世界卫生组织的194个成员国在2016年5月28日集体宣布,要在2030年前消灭乙型和丙型肝炎。对于那些乙型和丙型肝炎病毒肆虐的国家而言,这是一个相当艰巨的目标。中国和巴基斯坦都有超过1000万丙型肝炎患者,俄罗斯、乌克兰、巴西和阿根廷的患者虽然没有那么多,但也不少。
为了帮助近百个不发达国家对抗丙型肝炎,百时美施贵宝在2015年批准了一系列达卡他韦的仿制药生产许可协议。吉利德科学公司则以原价1%的价格将药物卖给这些国家,并允许十几家印度药厂生产仿制药。吉利德科学公司还与一些丙型肝炎疫情严重的国家达成了合作,例如有12%的人口患有丙型肝炎的埃及。在2014年,埃及启动了一项为国民免费提供丙型肝炎治疗的活动,到2016年大约有100万患者得到了治疗。格鲁吉亚是丙型肝炎感染率第三高的国家,感染人数占总人口的5%。在美国政府的支持下,格鲁吉亚政府于2015年在全国开展了一项免费治疗丙型肝炎的计划,所用药物就是由吉利德科学公司提供的。目前该国已经有超过2.4万名患者得到了治疗。但在其他国家,如巴西、中国,由于吉利德科学公司生产的索非布韦价格过于高昂,其专利申请遭到了拒绝。一些机构,如世界医生组织以及无国界医生组织甚至向欧洲专利局抗议其专利的合理性,希望可以通过这种手段促进丙型肝炎仿制药的出现。
要彻底消灭丙肝需要解决的其他难题还有:使所有患者都能迅速获得治疗的手段、在治疗结束后的3个月确认病毒消失的方法(这是治愈的标志)。最后,发展中国家特有的一个问题是医疗设备交叉使用造成的医源性感染。根据世界卫生组织的数据,全世界5%的医疗注射并不安全;如果把毒品注射也算在内,那么在2015年,这类注射共造成了175万个新的丙肝感染病例。
在不到10年内,DAA的发现就彻底改变了我们对抗丙型肝炎的斗争局势。全世界的卫生部门和政府管理机构会牢牢把握这个历史性的机遇,使普罗大众彻底摆脱这种致命的病毒感染吗?


