许多科幻小说和电影中都有将人体冷冻起来,到未来再解冻复苏的情节。然而,我们的科学技术尚未达到这种水平,目前能在冷冻条件下保存的只有单细胞(如胚胎细胞、卵细胞、精子等),而且需要冷冻在特殊试剂中。至于稍复杂的器官,则只能在低温条件(通常为4°C)下短期保存,如心脏能保存约4-6小时,肝脏约8-12小时,肾脏约24-30小时。
可是,偏偏就有这样一种生物,冬天时会冻成“冰块”,春天时又能融化苏醒。它就是木蛙(Rana sylvatica),这是一种在北美广泛分布的蛙类,也是唯一一种能在北极圈内生存的两栖动物。冷冻状态下,木蛙的心脏会停止跳动,大脑也会暂时歇业。极端情况下,木蛙最低能耐受-18°C的严寒,即便是冷冻7个月之久,气温升高后还依然能够正常复苏,活蹦乱跳,毫发无损。
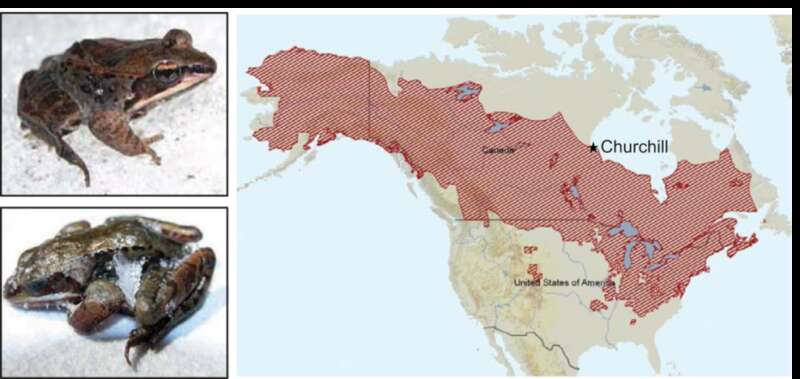
正常状态和冰冻的木蛙(左)及其分布范围(右)(图片来源:原论文)
机体冷冻后无损解冻之所以困难,是因为冷冻和解冻过程会对其造成不可逆的损伤。例如,在细胞外基质结冰的过程中,由于细胞外基质的水分结成了冰晶,溶质析出,所以细胞外基质的渗透压会逐渐升高,造成细胞内的水分转移到细胞外,使细胞脱水、体积减小;这些冰晶还会破坏细胞膜,以及细胞内的细胞器和细胞骨架。另外,血液凝固导致的局部缺血还会使组织缺氧坏死;而解冻过程又会促进活性氧(ROS)的产生,进一步损伤细胞。
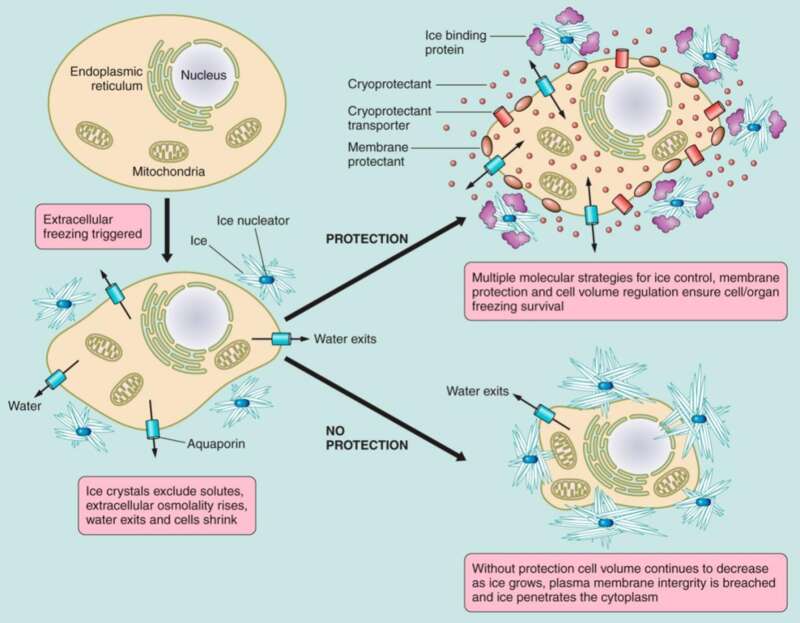
细胞外液结冰对细胞的影响(图片来源:原论文)
所以,在漫漫冬季,木蛙是如何避免这些损伤的呢?
冰冻的木蛙
1994年,研究人员利用核磁共振对冷冻和解冻过程中的木蛙进行成像,发现木蛙身体结冰和解冻的过程都很缓慢。结冰过程从身体边缘的肢体部位开始,以特定方向逐渐蔓延至身体内部。冷冻开始的2小时后(下图左D),木蛙的心脏已经结冰,停止了跳动,但肝脏却依然保持着未冻结的状态,不过体积大大减小。慢慢地,木蛙的肝脏也开始结冰,最终全身冻成冰块,整个过程持续4个多小时。
而解冻则是个完全相反的过程。当外界温度恢复到0°C以上,首先解冻的是木蛙的内脏,再向全身各方向蔓延开去。到52分钟(下图右C)时,木蛙的肝脏已经完全解冻,成为最先解冻的器官,不过肝脏的体积并没能恢复到原始状态。慢慢地,木蛙四肢的肌肉组织也开始解冻。3个小时过去后,木蛙的心脏才完全恢复,血液再次灌注到血管和肝脏之中。
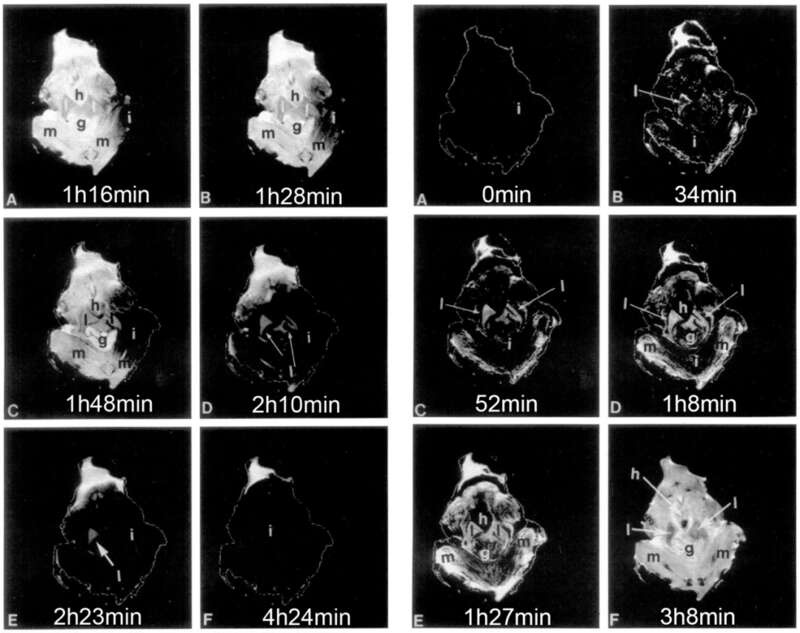
冷冻(左)和解冻(右)过程中的木蛙,黑色部位(i)表示结冰,“h”指示心脏,“l”指示肝脏(图片来源:原论文)
可见,肝脏在木蛙的耐冻特性中有着重要作用。科学家们发现,在夏季和秋季,木蛙会在肝脏中储备大量的肝糖原。到了冬季,当温度降低,它们的肝脏会开始快速分解肝糖原,产生大量葡萄糖。同时,木蛙的心率会快速上升,在结冰过程开始的1分钟内,木蛙的心率直接会翻一番,这有助于葡萄糖快速地分布到全身。
对于细胞来说,葡萄糖是一种很好的冷冻保护剂。而为了快速吸收血液大量的葡萄糖,木蛙的细胞从秋季开始,就会大量表达葡萄糖转运蛋白,并一直维持到冬季。这样当冬季来临,这些细胞就会高效地将葡萄糖转运至细胞内,避免细胞内部结冰。由于不同器官和组织对葡萄糖的摄取能力不同,最终,木蛙的大脑和腹部核心器官会获得更多葡萄糖,而骨骼肌和皮肤等外周组织中的葡萄糖浓度则相对较低。
与夏季的木蛙相比,秋冬季木蛙血浆和组织中的葡萄糖水平升高了50至80倍。要知道,正常人的空腹血糖水平低于5.0 mmol/L,而木蛙的冬季血糖水平可以达到高于200 mmol/L,是名副其实的“高血糖患者”。
除葡萄糖外,木蛙还会累积其它的抗冻分子,例如,从夏季到冬季,木蛙体内的尿素水平升高了10倍。这些分子和葡萄糖被细胞吸收后,会一起增加细胞内的渗透压,在避免胞内结冰的同时,减少细胞内的水分流失。
可是,除了细胞之外,木蛙身体的其他部分都会冻结,其体内65%-70%的水分都会结冰,仅仅避免细胞内不结冰还远远不够,还得让细胞外的冰晶不对细胞造成损伤。而木蛙采取了两种方式来应对这一难题。
首先,木蛙会表达专门的冷冻响应蛋白(Fr10),这种蛋白会在寒冷和细胞脱水、缺氧时高表达。这是一种冰结合蛋白,它能到达细胞外并和冰晶结合,最大限度地避免小冰晶再次结晶形成大冰晶,从而降低冰晶生长对细胞和组织造成的伤害。其次,木蛙还会在冬季改变细胞膜的组成成分,增加细胞膜的流动性,维持细胞膜的稳定。
不只是抗冻
由于冻结状态下的木蛙会停止呼吸,机体内的氧气会很快耗尽,细胞产生的能量会大大减少。所以,木蛙必须要在冬季数个月的时间内,将机体维持在低耗能的状态,诸如蛋白质合成、细胞分裂等细胞活动都需要维持在最低限度,同时还要维持生存必要的活动,例如抗氧化、抗细胞凋亡、基础的免疫功能等等。
为了抑制机体的代谢,木蛙一方面会通过表观遗传学的方式,通过DNA修饰和转录因子的调节,下调某些基因的表达。例如,由于氧气缺失,细胞只能以无氧呼吸方式供能,木蛙就会下调线粒体相关基因(参与有氧呼吸)的表达,这同时能减少对细胞有害的活性氧的产生。
另一方面,木蛙还会表达特定的microRNA,在一些基因正常转录后,限制并大大减少后续蛋白质的合成。这些用于调控的microRNA会在冷冻时显著增加,而解冻时显著减少,蛋白质的合成就会快速恢复,这样木蛙能在冷冻/解冻两种状态之间的实现切换。对于合成出来的蛋白质,木蛙也会通过翻译后修饰(PTM)稳定或增加它们的活性,让它们在代谢抑制的状态下能正常工作。
同样地,也是利用这些方式,木蛙上调了凝血和抗氧化应激相关基因的表达和相关蛋白的稳定性及活性。这样,即便机体内不幸出现的大冰晶造成了组织损伤和出血,木蛙也能迅速修复这些伤害。也能在春天到来,体内的冰晶融化时,尽量减少氧化应激带来的危害。
可是,停止呼吸带来的问题远不止能量供应受限。你也许知道,长时间剧烈运动,肌肉细胞的无氧呼吸会累积大量乳酸,严重时甚至会造成乳酸酸中毒。木蛙面临的是每年好几个月的无氧呼吸。因此,木蛙会调整部分组织中的代谢通路。在无氧呼吸中,乳酸主要由丙酮酸转化形成。木蛙通过将丙酮酸更多地用于合成丙氨酸,减少了乳酸的累积,最大限度地避免组织中的乳酸酸中毒。
科幻小说或许能成真
极寒地带生活着许多动物,木蛙是其中少见的、以冷冻机体的方式过冬的生物,其它生物通常会避免体内结冰。一般来说,动物们会运用两种策略:一是产生抗冻蛋白或如甘油类的冷冻保护剂,以维持机体内水分的过冷状态,例如陆生节肢动物通常会以这种方式应对寒冷;二是让机体低温脱水,例如水熊虫一类的缓步动物采取的就是这种方式。

水熊虫(图片来源:维基百科)
科学家们也一直在从这些生物的抗冻机制中汲取灵感。例如,他们已经能利用葡萄糖的类似物,把大鼠肝脏的冷冻保存时间延长到96小时;通过一些小分子来抑制细胞的代谢,使得冷冻又复苏的细胞的活力得以保持,DNA损伤也大大减少。这些工作不仅能给那些想冷冻身体看看未来世界的人们带来希望,还会极大地推动再生医学和器官移植等学科的发展。
随着全球气候的变暖,木蛙原本用来度过冬季的机制或许会在未来的某一天成为历史。至于在无法靠冰冻自己度日的冬天里,它们能否找到充足的食物,又会以怎样的方式去应对新的气候挑战,就有待更多科学家们的研究了。